堿性燃料電池(alkalinefuelcell,AFC)是一種燃料電池,由法蘭西斯·湯瑪士·培根(FrancisThomasBacON)所發(fā)明,以碳為電極,并使用氫氧化鉀為電解質(zhì)。堿性燃料電池的電能轉(zhuǎn)換效率為所有燃料電池中最高的,最高可達(dá)70%。
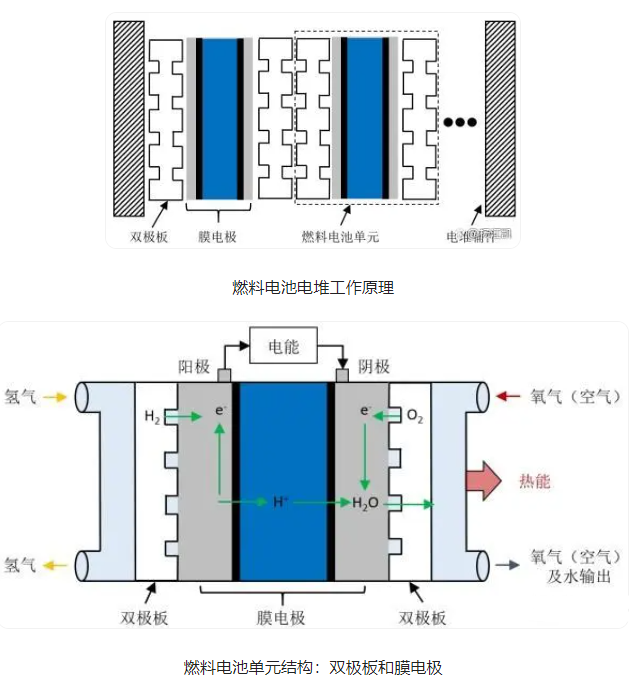
堿性燃料電池的工作原理
氫氧燃料電池有兩個(gè)燃料入口,氫及氧各由一個(gè)入口進(jìn)入電池,中間則有一組多孔性石墨電極,電解質(zhì)則位于碳陰極及碳陽(yáng)極中央。氫氣經(jīng)由多孔性碳陽(yáng)極進(jìn)入電極中央的氫氧化鉀電解質(zhì),在接觸后進(jìn)行氧化,產(chǎn)生水及電子。
H2+2OH-→2H2O+e-
電子經(jīng)由外電路提供電力并流回陰極,并在陰極與氧及水接觸后反應(yīng)形成氫氧根離子
O2+2H2O+4e-→4OH-
最后水蒸汽及熱能由出口離開(kāi),氫氧根離子經(jīng)由氫氧化鉀電解質(zhì)流回陽(yáng)極,完成整個(gè)電路。
堿性燃料電池的反應(yīng)原理
堿性燃料電池通常用氫氧化鉀或氫氧化鈉為電解質(zhì),導(dǎo)電離子為OH-,燃料為氫。
陽(yáng)極反應(yīng):H2+2OH-→2H2O+O2標(biāo)準(zhǔn)電極電位為-0.0828V
陰極反應(yīng):1/2O2+H2O+2e-→2OH-標(biāo)準(zhǔn)電極電位為0.401V
總反應(yīng):1/2O2+O2+H2→H2O理論電動(dòng)勢(shì)為0.401-(-0.828)=-1.229V
AFC的催化劑主要用貴金屬鉑、鈀、金、銀和過(guò)渡金屬鎳、鈷、錳等。
-
燃料電池
+關(guān)注
關(guān)注
26文章
967瀏覽量
95396 -
電池
+關(guān)注
關(guān)注
84文章
10679瀏覽量
131337
發(fā)布評(píng)論請(qǐng)先 登錄
相關(guān)推薦
海瑞思助力氫燃料電池檢測(cè)效率提升
燃料電池測(cè)試負(fù)載如何進(jìn)行負(fù)載測(cè)試?
燃料電池技術(shù)的環(huán)保優(yōu)勢(shì)
燃料電池與氫氣的關(guān)系 燃料電池與電動(dòng)汽車的比較
燃料電池在可再生能源中的應(yīng)用
燃料電池的主要材料 燃料電池的效率和性能
燃料電池的應(yīng)用領(lǐng)域 燃料電池車的優(yōu)缺點(diǎn)
燃料電池工作原理 燃料電池與傳統(tǒng)電池的區(qū)別
燃料電池測(cè)試負(fù)載的工作原理是什么?
燃料電池質(zhì)子交換膜透氣性測(cè)試儀

什么是燃料電池?燃料電池和動(dòng)力電池區(qū)別
燃料電池的特點(diǎn)及應(yīng)用
燃料電池工作原理與結(jié)構(gòu) 燃料電池并網(wǎng)和光伏發(fā)電并網(wǎng)區(qū)別




 堿性燃料電池的工作原理_堿性燃料電池的反應(yīng)原理
堿性燃料電池的工作原理_堿性燃料電池的反應(yīng)原理










評(píng)論