醫(yī)用高分子材料按照用途,可分為心血管系統(tǒng)、軟組織及硬組織等修復(fù)材料等。這些材料除應(yīng)滿足一般的物理、化學(xué)性能要求外,還必須具有足夠好的生物相容性,例如,用于心血管系統(tǒng)的醫(yī)用高分子材料應(yīng)當著重要求其抗凝血性好,不破壞紅細胞、血小板,不改變血液中的蛋白并不干擾電解質(zhì)等。
以大幅度改善生物醫(yī)用材料與生物體的相容性為目標,北京市生物醫(yī)學(xué)工程高精尖創(chuàng)新中心常凌乾教授與浙江工業(yè)大學(xué)陳楓副教授、浙江大學(xué)附屬第二醫(yī)院劉震杰副主任醫(yī)師合作,結(jié)合紫外光引發(fā)和巰基“click”聚合兩種方法,使用光影印法制備了一系列力學(xué)性能優(yōu)異、無毒無污染、生物可降解的微米級表面圖案化高分子材料。
聯(lián)合團隊前期已經(jīng)在傳統(tǒng)生物惰性材料上驗證了技術(shù)可行性,實現(xiàn)在生物惰性PDMS表面上,紫外光引發(fā)巰基“click”固定修飾具有生物活性的聚多巴胺(PDA)納米微球。通過調(diào)控PDA的微觀聚集形貌(納米微球或光滑薄膜),賦予PDMS材料表面pH響應(yīng)的的親/疏水、蛋白質(zhì)吸/脫附表面摩擦系數(shù)改變;同時大幅改善細胞在材料表面的生長情況(ACS Appl. Bio Mater., 2018, 1(6): 2167-2175)。并采用紫外光引發(fā)和巰基“click”聚合制備高精度3維血管支架,相比較商用光固化樹脂體系(PEGDMA),反應(yīng)樹脂體系無有機溶劑和光引發(fā)劑,光固化材料無小分子殘留,生物相容性好,拉伸強度高,柔韌性好,成型精度高(Chem. Eng. J., 2019, 366: 112-122),并申請發(fā)明專利2項。
近期,合作團隊將該方法拓展至快速制備3維成型生物可降解水凝膠。透明質(zhì)酸(HA)是組織工程支架材料的優(yōu)異選擇。但由于透明質(zhì)酸粘度大、吸水性強,在高精度成型領(lǐng)域研究領(lǐng)域,尤其是微納米圖案化結(jié)構(gòu)的透明質(zhì)酸水凝膠存在重大材料和技術(shù)挑戰(zhàn)。合作團隊選擇高分子量透明質(zhì)酸前體,分子鏈經(jīng)過雙鍵改性,與水溶性四半胱氨酸交聯(lián)劑復(fù)配成水溶液,在波長405納米紫外光輻照下,快速固化為無毒無小分子污染、體內(nèi)可降解的透明質(zhì)酸水凝膠,其含水量可達95 wt%以上。
圖1. 透明質(zhì)酸水凝膠結(jié)構(gòu)和性能:a)冷凍干燥后透明質(zhì)酸凝膠網(wǎng)絡(luò)結(jié)構(gòu);b)凝膠表面20微米流道形貌;以及不同交聯(lián)劑含量的凝膠c)固化時間、d)拉伸強度和e)壓縮強度。
隨著四半胱氨酸交聯(lián)劑用量的調(diào)整,透明質(zhì)酸水凝膠的固化時間和力學(xué)性能均可以大幅度調(diào)整,在1 wt %交聯(lián)劑用量條件下,透明質(zhì)酸水凝膠紫外固化成型時間小于60秒,拉伸強度可達0.65 kPa,壓縮強度可提升至69.28 kPa。合作團隊采用光影印法,成功制備精度為10微米的透明質(zhì)酸圖案化表面。
圖2. a)透明質(zhì)酸水凝膠在小鼠體內(nèi)1周、2周和4周后植入降解情況:A小鼠體內(nèi)H&E染色照片;B凝膠表面CD3淋巴細胞增殖情況。b)凝膠培養(yǎng)HUVEC細胞后p-FAK和FAK蛋白印跡,以及 c)不同交聯(lián)度凝膠的 VEGF釋放量。d)不同交聯(lián)度凝膠體外降解實驗。
進一步,團隊系統(tǒng)研究了透明質(zhì)酸水凝膠負載VEGF后的體外可控釋放、內(nèi)皮細胞培養(yǎng)和小鼠體內(nèi)生物相容性試驗。證明了較低交聯(lián)度的透明質(zhì)酸水凝膠具有適中的VEGF釋放速率,透明質(zhì)酸水凝膠擁有優(yōu)異的細胞相容性,即使是高交聯(lián)度水凝膠樣品植入在小鼠體內(nèi)三至四周后也已完全降解。
該工作近期發(fā)表在Journal of Materials Chemisry B上(DOI: 10.1039/C9TB02796C),并被選為內(nèi)頁封面論文。張倩敏碩士和季永麗博士為論文共同第一作者,陳楓副教授、劉震杰副主任醫(yī)師和常凌乾教授為論文共同通訊作者。以上系列工作受到國家自然科學(xué)基金、浙江省自然科學(xué)基金、浙江省衛(wèi)生廳項目和北京市生物醫(yī)學(xué)工程高精尖創(chuàng)新中心經(jīng)費資助。
常凌乾教授課題組:研究方向主要包括生物納米技術(shù)、生物芯片和生物納米材料。已在國際期刊發(fā)表SCI論文50余篇,包括Nature Nanotechnology, Nano Letters, Small等。已申請和授權(quán)美國專利3項,中國專利9項。主編英文專著1部(Springer),書章節(jié)3章。獲得了諸多科研獎勵和榮譽,如俄亥俄州立大學(xué)博士最高獎Presidential Fellowship,北德克薩斯大學(xué)RSG Awards, MINE 2018‘杰出青年科學(xué)家’提名獎等。入選2017年中組部‘千人計劃’青年項目。現(xiàn)任SCI期刊Biomedical Engineering Online副主編(Associate Editor)和Computers in Biology and Medicine編委(Editorial Board), Springer Nature《Electroporation Protocol》第三版主編。
-
生物醫(yī)學(xué)
+關(guān)注
關(guān)注
0文章
46瀏覽量
11185 -
微納米
+關(guān)注
關(guān)注
0文章
20瀏覽量
7579
原文標題:微納米光影印法工藝綠色制備高分子生物材料及其在生物醫(yī)學(xué)工程中的應(yīng)用
文章出處:【微信號:MEMSensor,微信公眾號:MEMS】歡迎添加關(guān)注!文章轉(zhuǎn)載請注明出處。
發(fā)布評論請先 登錄
相關(guān)推薦
三大電功能高分子材料介紹
高分子微納米功能復(fù)合材料3D打印加工介紹

DFT在生物信號分析中的應(yīng)用
高分子半導(dǎo)體的特性與創(chuàng)新應(yīng)用探索
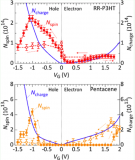
功率放大器應(yīng)用:超聲波換能器從材料策略到生物醫(yī)學(xué)的應(yīng)用

安泰功率放大器應(yīng)用領(lǐng)域:微流控技術(shù)和分子結(jié)合的體外診斷研究
高通量生物分析技術(shù)之微流控芯片
微流控芯片行業(yè)市場規(guī)模及未來前景預(yù)測
搪瓷釜脫瓷嚴重漏介質(zhì),用高分子復(fù)合材料輕松修補

新型材料在生物檢測方面的應(yīng)用和前景

北卡羅來納州立大學(xué):加速外骨骼機器人控制系統(tǒng)的研發(fā)
電化學(xué)生物傳感器在生物檢測領(lǐng)域的顯著優(yōu)勢
綜述:基于微流控技術(shù)的氧釋放生物材料的制備與應(yīng)用研究進展
Aigtek安泰電子第一屆全國等離子體生物醫(yī)學(xué)學(xué)術(shù)會議圓滿結(jié)束!





 微納米光影印法工藝綠色制備高分子生物材料及其在生物醫(yī)學(xué)工程中的應(yīng)用
微納米光影印法工藝綠色制備高分子生物材料及其在生物醫(yī)學(xué)工程中的應(yīng)用










評論