核酸分子具有豐富的遺傳信息,對(duì)疾病診斷具有關(guān)鍵價(jià)值。傳統(tǒng)核酸檢測(cè)技術(shù)受限于耗時(shí)長(zhǎng)、需大型儀器設(shè)備等局限,嚴(yán)重制約了其在大規(guī)模、突發(fā)性疾病檢測(cè)中的應(yīng)用。紙基微流控具有便攜、自驅(qū)動(dòng)等優(yōu)勢(shì),在整合等溫?cái)U(kuò)增技術(shù)后,為核酸分子快速、準(zhǔn)確的檢測(cè)提供可能。
據(jù)麥姆斯咨詢報(bào)道,近期,來(lái)自重慶大學(xué)等科研機(jī)構(gòu)的研究人員,于《重慶醫(yī)科大學(xué)學(xué)報(bào)》發(fā)表綜述文章,從紙基微流控的設(shè)計(jì)出發(fā),總結(jié)了紙基微流控在核酸分子檢測(cè)中的研究進(jìn)展,并分析了影響其檢測(cè)靈敏度、穩(wěn)定性等的干擾因素,為推動(dòng)紙基微流控向臨床轉(zhuǎn)化提供重要參考。
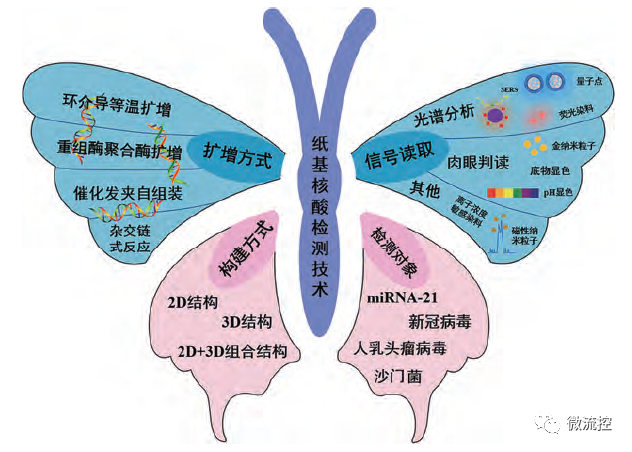
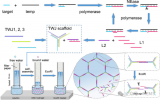
圖1 基于紙基微流控的核酸檢測(cè)技術(shù)
基于環(huán)介導(dǎo)等溫?cái)U(kuò)增(LAMP)的紙基核酸快速檢測(cè)
LAMP體系中Mg2?、焦磷酸等副產(chǎn)物的變化常被作為核酸檢測(cè)依據(jù)。為與紙基微流控更好地整合,基于體系中Mg2?的濃度變化,有研究人員利用多層紙基材料進(jìn)行3D組裝,結(jié)合蠟染技術(shù)構(gòu)建了多個(gè)具有縱向流體空間的LAMP反應(yīng)區(qū)(圖2A),僅需一步加樣,即可通過(guò)Mg2?敏感染料羥基萘酚藍(lán)的熒光特性對(duì)LAMP信號(hào)進(jìn)行實(shí)時(shí)分析。此外,利用LAMP擴(kuò)增過(guò)程中能產(chǎn)生大量焦磷酸,導(dǎo)致反應(yīng)體系的pH發(fā)生明顯改變這一特點(diǎn)的紙基pH指示法,已在寨卡病毒等檢測(cè)中被證明具有較高靈敏度,檢測(cè)限低至1拷貝/μL。除了利用LAMP反應(yīng)體系本身的特性變化作為檢測(cè)依據(jù)外,其他報(bào)道的紙基LAMP信號(hào)輸出方法還包括底物顯色、熒光標(biāo)記和基于流體層析距離(圖2B)的檢測(cè)等。然而,上述研究大多依靠單獨(dú)的擴(kuò)增步驟。為將擴(kuò)增與檢測(cè)整合于一體,有研究人員設(shè)計(jì)了一種瘧疾檢測(cè)POCT裝置(圖2C),并通過(guò)整合一個(gè)多功能3D紙帶進(jìn)行臨床血液樣本的擴(kuò)增前預(yù)處理;經(jīng)LAMP反應(yīng)后,靶標(biāo)能繼續(xù)與通道中預(yù)儲(chǔ)存的紅色微球結(jié)合,隨后在2D紙基微流控上完成檢測(cè),實(shí)現(xiàn)了擴(kuò)增與檢測(cè)一體化。
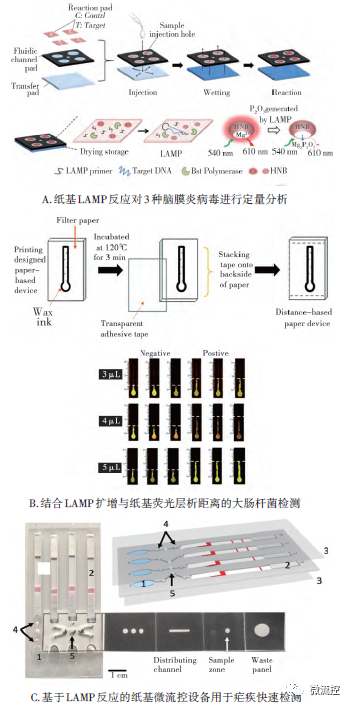
圖2 基于LAMP技術(shù)的紙基核酸快速檢測(cè)
基于重組酶聚合酶擴(kuò)增(RPA)的紙基核酸快速檢測(cè)
與LAMP相比,RPA技術(shù)能夠在37℃的室溫條件下在20mi內(nèi)實(shí)現(xiàn)靶核苷酸的高效常溫?cái)U(kuò)增。由于RPA具有相對(duì)較低的最適擴(kuò)增溫度,因此在選擇疏水區(qū)構(gòu)建方法時(shí)無(wú)須考慮反應(yīng)溫度對(duì)疏水材料的影響,便于直接在紙基微流控上實(shí)現(xiàn)擴(kuò)增與檢測(cè)一體化。
基于雜交鏈?zhǔn)椒磻?yīng)(HCR)的紙基核酸快速檢測(cè)
HCR是一種無(wú)酶核酸擴(kuò)增技術(shù),該技術(shù)的提出使得核酸分子的體外擴(kuò)增擺脫了對(duì)聚合酶的依賴,進(jìn)一步降低了紙基核酸快速檢測(cè)裝置的生產(chǎn)、存儲(chǔ)成本。目前,已有相關(guān)研究利用HCR反應(yīng)設(shè)計(jì)了一種能更高效檢測(cè)沙門菌的紙基微流控芯片(圖3A)。此外,有研究人員在基于HCR反應(yīng)的同時(shí)巧妙地利用了紙張的咖啡環(huán)效應(yīng)作為信號(hào)轉(zhuǎn)導(dǎo)手段(圖3B),將體系中液體的蒸發(fā)過(guò)程轉(zhuǎn)化為紙張末端彩色條帶的形成過(guò)程,僅需測(cè)量著色帶長(zhǎng)度即可對(duì)miRNA-21進(jìn)行定量,檢測(cè)限為0.2pmol/L,為提高檢測(cè)靈敏度提供了新思路。
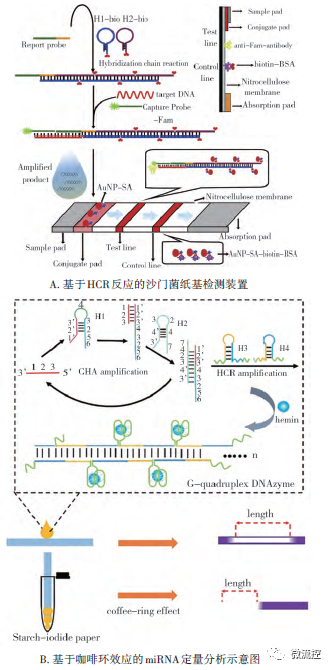
圖3 基于HCR 技術(shù)的紙基核酸快速檢測(cè)
基于催化發(fā)卡自組裝反應(yīng)(CHA)的紙基核酸快速檢測(cè)
CHA是在HCR技術(shù)基礎(chǔ)上開(kāi)發(fā)的一種更高效、更靈敏的無(wú)酶信號(hào)放大技術(shù)。CHA與HCR的主要區(qū)別在于,CHA反應(yīng)中靶標(biāo)觸發(fā)級(jí)聯(lián)放大效應(yīng)后并不會(huì)作為生成物的一部分參與后續(xù)延伸,而是會(huì)被重新釋放到體系中充當(dāng)“催化劑”繼續(xù)觸發(fā)下一段CHA反應(yīng),產(chǎn)生更明顯的信號(hào)放大效果。無(wú)酶催化的CHA具有更高靈敏度和放大效率,在紙基微流控中是一種同樣經(jīng)濟(jì)且更適用于微量靶標(biāo)的檢測(cè)手段。
基于CHA反應(yīng)強(qiáng)大的信號(hào)放大效果,研究人員開(kāi)發(fā)了一種能夠在紙質(zhì)芯片上具有雙重放大能力的早期胰腺癌診斷卡(圖4A)。與傳統(tǒng)的免疫分析試紙條相比,該設(shè)計(jì)通過(guò)同時(shí)引入CHA和金沉積手段達(dá)到更高的檢測(cè)靈敏度。為了縮短反應(yīng)時(shí)間、提高檢測(cè)效率,研究人員進(jìn)一步將該技術(shù)進(jìn)行了拓展:在靶標(biāo)觸發(fā)CHA反應(yīng)后,分別利用量子點(diǎn)和多色熒光基團(tuán)標(biāo)記取代了金增強(qiáng)步驟(圖4B-C),實(shí)現(xiàn)對(duì)miRNA-21和丙型肝炎病毒精確定量的同時(shí)將反應(yīng)時(shí)間縮短至原來(lái)的1/3。
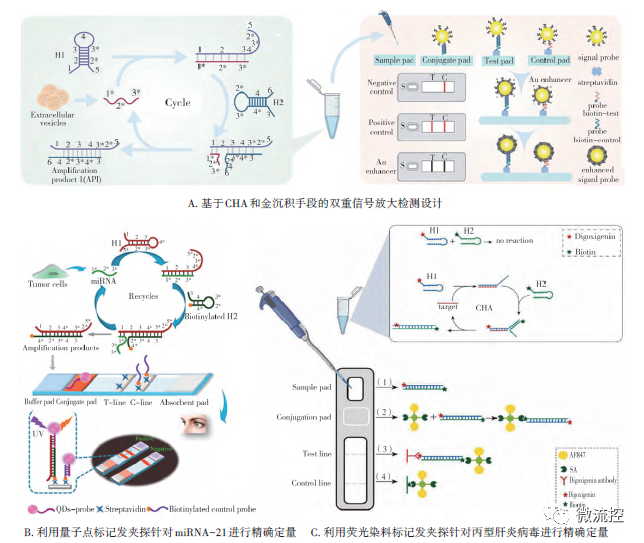
圖4 基于CHA技術(shù)的紙基核酸快速檢測(cè)
總體而言,紙基微流控技術(shù)自21世紀(jì)初研發(fā)以來(lái)取得了巨大進(jìn)步,已成為臨床POCT領(lǐng)域的重要組成部分。隨著研究的深入,其在核酸快速檢測(cè)領(lǐng)域的檢測(cè)靈敏度、功能集成度等方面取得了較大突破;加之便攜式信號(hào)分析設(shè)備開(kāi)發(fā)以及機(jī)器學(xué)習(xí)等算法的引入正在逐步提高紙基微流控在核酸檢測(cè)中的定量分析能力,并逐步向智能化、通用化邁進(jìn)。近年來(lái)系列核酸等溫?cái)U(kuò)增技術(shù)被相繼開(kāi)發(fā)后,核酸擴(kuò)增擺脫了梯度溫控設(shè)備的限制,紙基微流控核酸檢測(cè)技術(shù)也因此迎來(lái)了高速發(fā)展。但用于核酸檢測(cè)的紙基微流控裝置在進(jìn)行臨床或復(fù)雜環(huán)境下的評(píng)估之前,必須在實(shí)驗(yàn)室進(jìn)行大量的測(cè)試和改良工作,以應(yīng)對(duì)真實(shí)應(yīng)用場(chǎng)景下可能出現(xiàn)的各種問(wèn)題。此外,將核酸檢測(cè)涉及的多個(gè)樣本預(yù)處理步驟集成在紙質(zhì)設(shè)備中,將難以避免地提升裝置的復(fù)雜程度,在此情況下如何同時(shí)方便用戶使用的問(wèn)題也不容忽視。
審核編輯:郭婷
-
機(jī)器學(xué)習(xí)
+關(guān)注
關(guān)注
66文章
8438瀏覽量
133086
原文標(biāo)題:綜述:基于紙基微流控的核酸分子快速檢測(cè)技術(shù)研究進(jìn)展
文章出處:【微信號(hào):Micro-Fluidics,微信公眾號(hào):微流控】歡迎添加關(guān)注!文章轉(zhuǎn)載請(qǐng)注明出處。
發(fā)布評(píng)論請(qǐng)先 登錄
相關(guān)推薦
測(cè)長(zhǎng)機(jī)能檢測(cè)螺紋環(huán)規(guī)嗎?
中國(guó)開(kāi)發(fā)出基于可編程DNA水凝膠的紙基比距傳感器
谷景科普如何檢測(cè)環(huán)形磁環(huán)電感好壞
使用OPT4003-Q1環(huán)境光傳感器進(jìn)行光源檢測(cè)

熒光檢測(cè)器適用范圍有哪些
變頻器參數(shù)的電流環(huán)速度環(huán)該如何調(diào)節(jié)?
谷景教你如何快速辨別儲(chǔ)能磁環(huán)電感的質(zhì)量好壞
4260紙機(jī)烘缸軸磨損是如何解決的
通用變頻器怎么進(jìn)行位置檢測(cè)?
紙機(jī)烘缸軸磨損的修復(fù)
快速控制原型RCP與硬件在環(huán)仿真HIL該如何區(qū)分呢?




 基于環(huán)介導(dǎo)等溫?cái)U(kuò)增的紙基核酸快速檢測(cè)
基于環(huán)介導(dǎo)等溫?cái)U(kuò)增的紙基核酸快速檢測(cè)










評(píng)論