化學動力療法(CDT)是一種采用芬頓催化劑將過氧化氫(H?O?)轉化為有毒的羥基自由基(?OH)來殺死細菌的方法。其中,芬頓金屬過氧化物納米顆粒是一種具有獨特物理化學性質的納米材料,但對這種抗菌劑的研究仍處于起步階段。
近日,來自青島科技大學的朱之靈副教授、隋凝副教授共同開發了一種獨特的異質結構,由超細過氧化物銅(CuO?)納米團簇和聲敏化超薄富氧空位多孔氧化鈦(OV- TiO?)納米片組成,并將其納入微針中,用于雙側增強聲化學動力學和聲溫抗菌治療(圖1)。該CuO?/TiO?集成微針(CTMN)貼片在體外和體內實驗中均有較好的效果,5 min內對多藥耐藥(MDR)病原體的去除率為》 99.9999%,并能促進創面組織愈合。
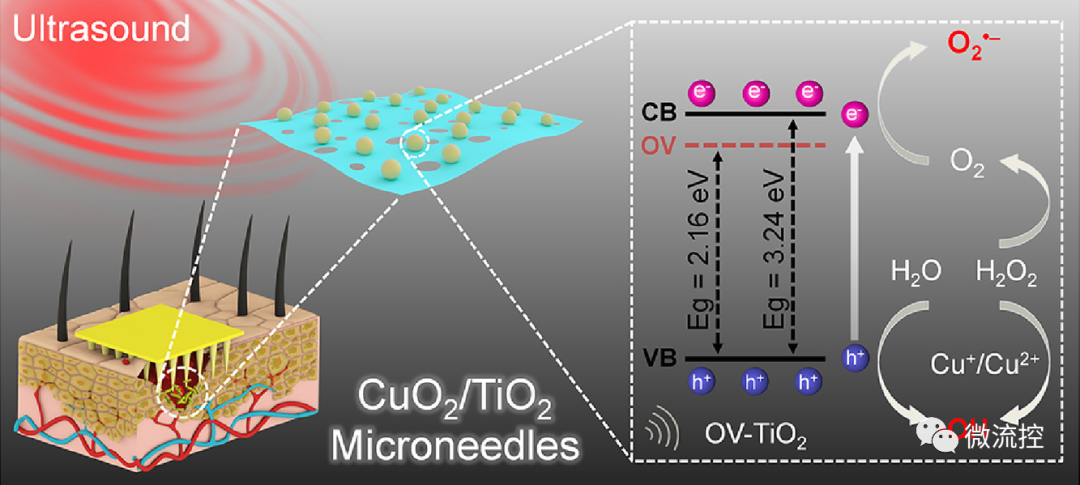
圖1 雙側增強聲化學動力學和聲溫抗菌治療的示意圖 相關研究成果以“Ultrasound Activatable Microneedles for Bilaterally Augmented Sono-Chemodynamic and Sonothermal Antibacterial Therapy”為題于近期發表在Acta Biomater.期刊上。
CuO?/TiO?的制備與表征
首先,研究人員按照一定的流程成功制備了CuO?/TiO?異質結構,并對其進行了相關表征(圖2A)。通過TEM和AFM探究了材料的形貌,利用XRD對其結構特征進行了進一步的分析。通過XPS的詳細分析對其表面的化學組成各元素的化學狀態進行了詳細分析(圖2I-L)。
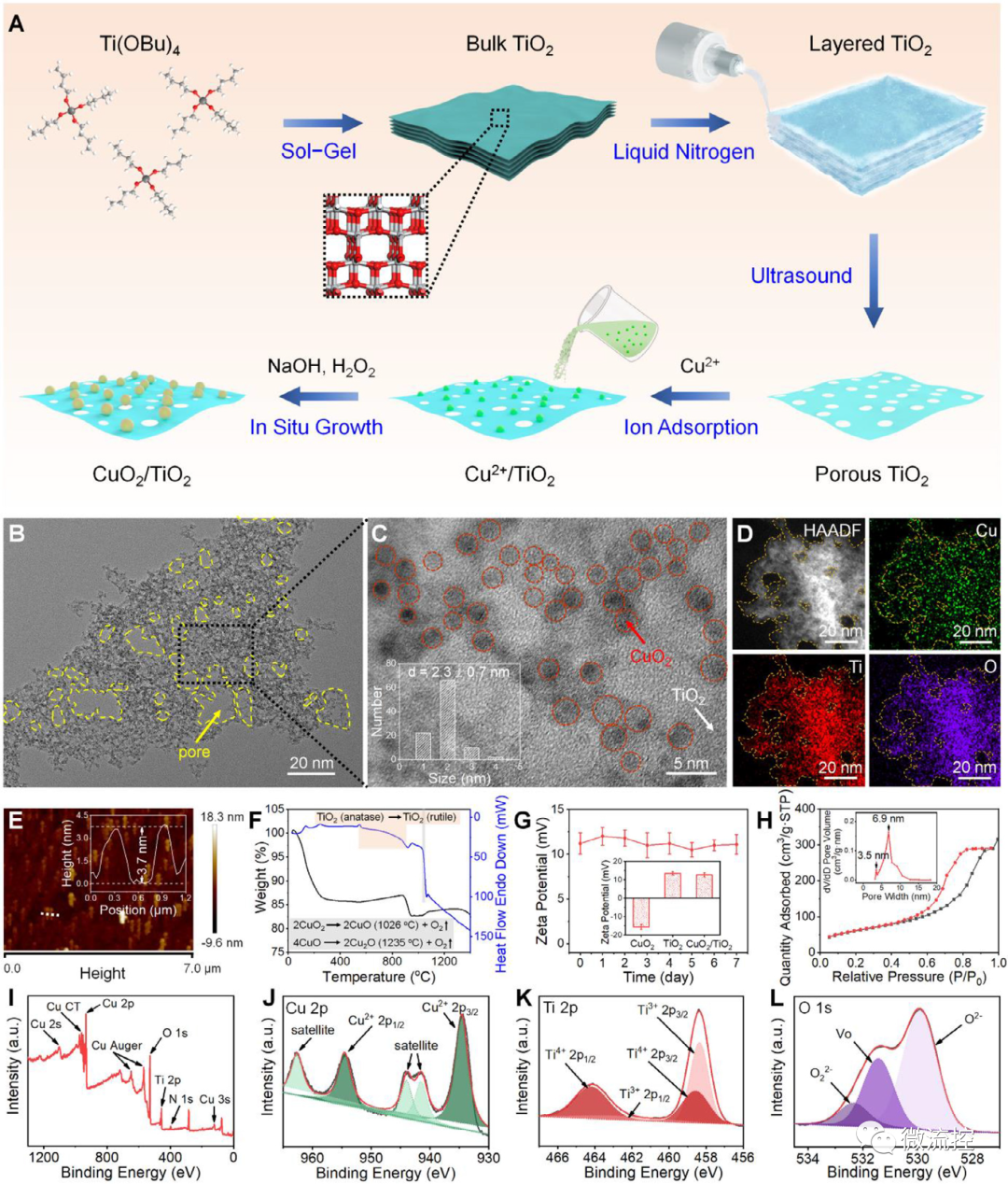
圖2 CuO?/TiO?的制備與表征
CuO?/TiO?的催化機理
隨后,經過一系列的測試和模擬,研究人員探索了聲動力增強ROS產生的可能機理。一方面,超聲作用于CuO?/TiO?時,CuO?分解,Cu2?釋放并吸附在TiO?表面,氧空位的存在減小了TiO?的帶隙,使得電子更容易從TiO?的價帶(VB)躍遷到TiO?的導帶(CB)上,提高了載流子遷移率。同時,Cu2?的存在可以促進芬頓反應,產生ROS自由基,殺死細菌。另一方面,當超聲波通過液體介質時,由于空化作用形成了大量的空化微泡,大量的能量聚集在這些空化微泡中。當液泡破裂時,大量的能量瞬間釋放出來,導致周圍的H?O分子斷裂,產生大量的?OH,從而殺死細菌。
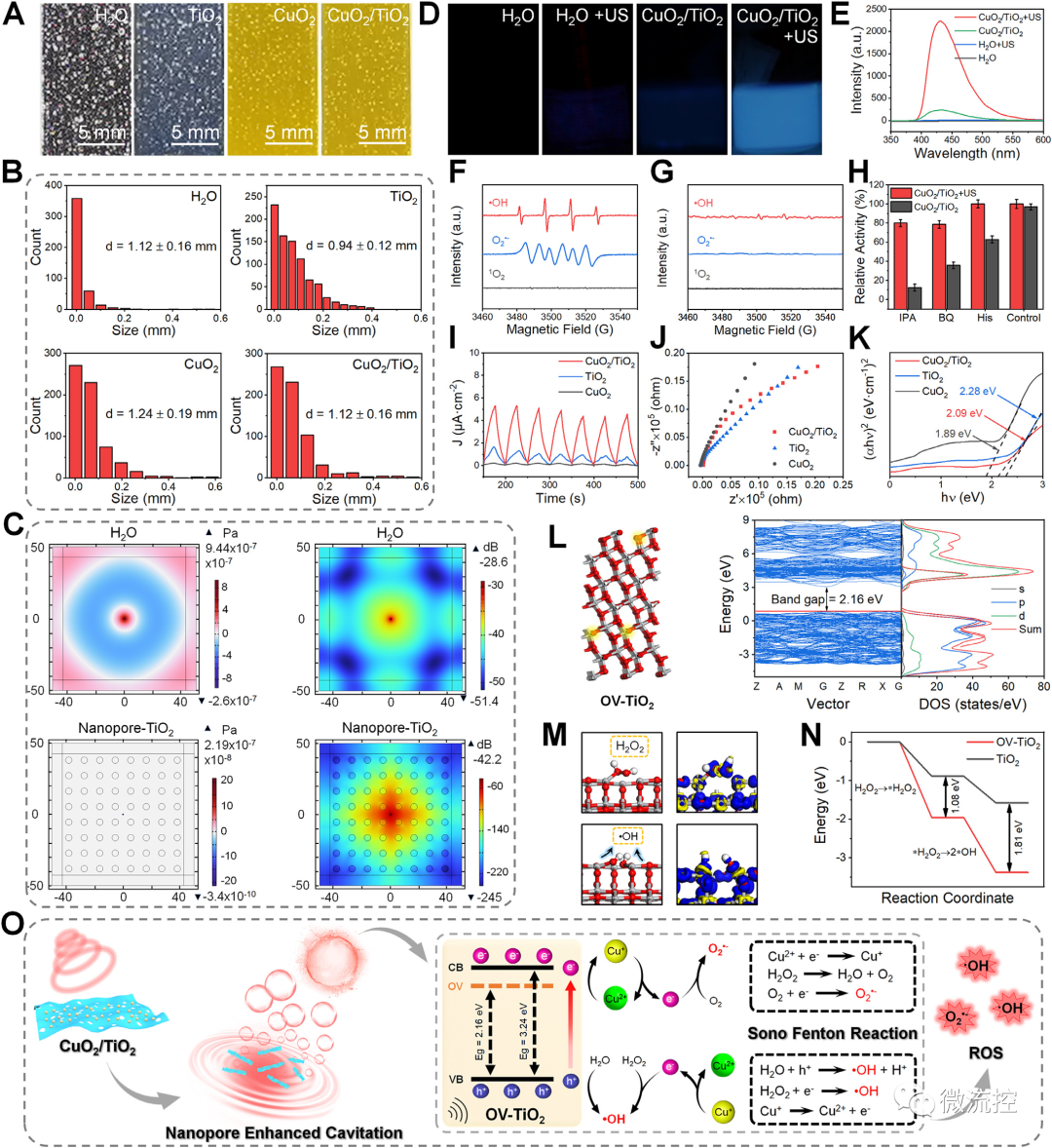
圖3 CuO?/TiO?的催化機理
CuO?/TiO?的體外抗菌性能
接著,采用革蘭氏陽性MRSA和革蘭氏陰性P. aeruginosa兩種耐多藥菌株對CuO?/TiO?的體外抗菌性能進行了評估(圖4)。結果顯示,無論是否應用超聲,TiO?組和對照組的菌落都沒有明顯減少。未超聲CuO?組菌落大量生長,超聲處理后菌落明顯減少。相比之下,未超聲CuO?/TiO?組僅形成少量菌落,而CuO?/TiO? + US組幾乎沒有菌落生長。
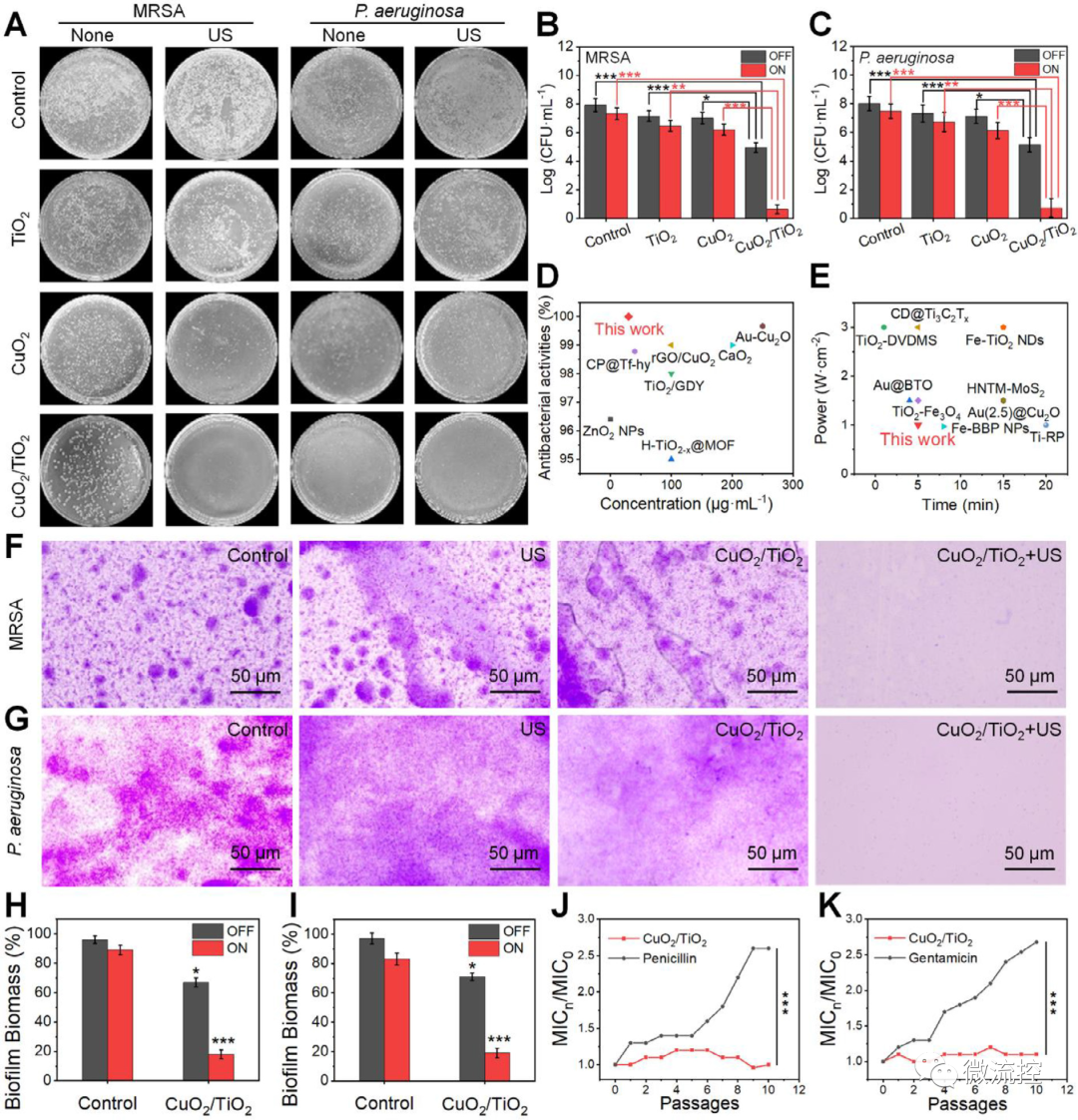
圖4 體外抗菌性能
為了揭示CuO?/TiO?的抗菌機制,研究人員檢測了處理后細菌的形態變化、膜完整性和細胞內ROS水平(圖5)。CuO?/TiO?細菌的強相互作用是由于CuO?/TiO?具有較大的比表面積和正電荷特性。與未處理細菌的正常光滑表面相比,CuO?/TiO?處理的細菌表面顯示出明顯的皺紋和收縮,這是超聲誘導脫水的結果。各組均未觀察到明顯的細菌膜損傷。實驗結果表明,非物理因素,特別是氧化應激和熱,是細菌死亡的主要原因。
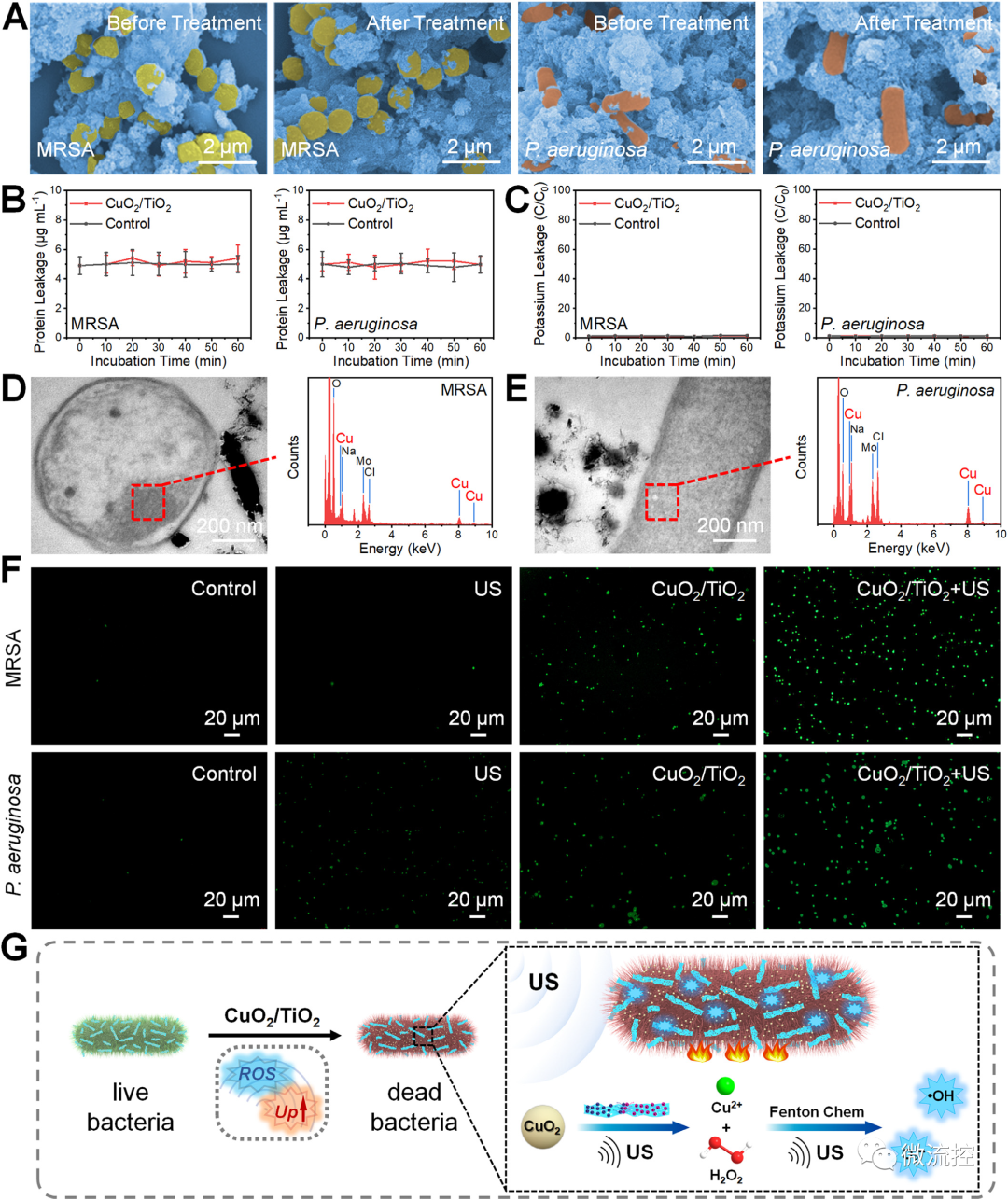
圖5 抗菌機理的探究
CuO?/TiO?微針(CTMN)的制備與表征
將分散體與HA溶液混合,然后在20 × 20微針陣列模具中固化,得到CuO?/TiO?集成微針(CTMN)。尖銳的針尖高度為600微米,間距為600微米,同時評估了CTMN的釋放動力學(圖6)。為了更好地觀察穿刺效果,使用豬皮體外研究了CTMN的皮膚插入能力。加壓5分鐘后,CTMN溶解并消失(圖6i),來自負載亞甲藍(MB)的CTMN的藍點保留在豬尸體皮膚中(圖6j)。此外,將處理過的豬尸體皮膚切片用蘇木精和曙紅(H&E)染色,染色結果表明CTMN穿透表皮并到達真皮。此后,在小鼠背部皮膚上進行體內皮膚插入試驗。負載異硫氰酸熒光素(FITC)的CTMN保留在背部皮膚的微通道中(圖6l),證實了CTMN可以穿透小鼠皮膚的真皮層并遞送CuO?/TiO?傷口部位。
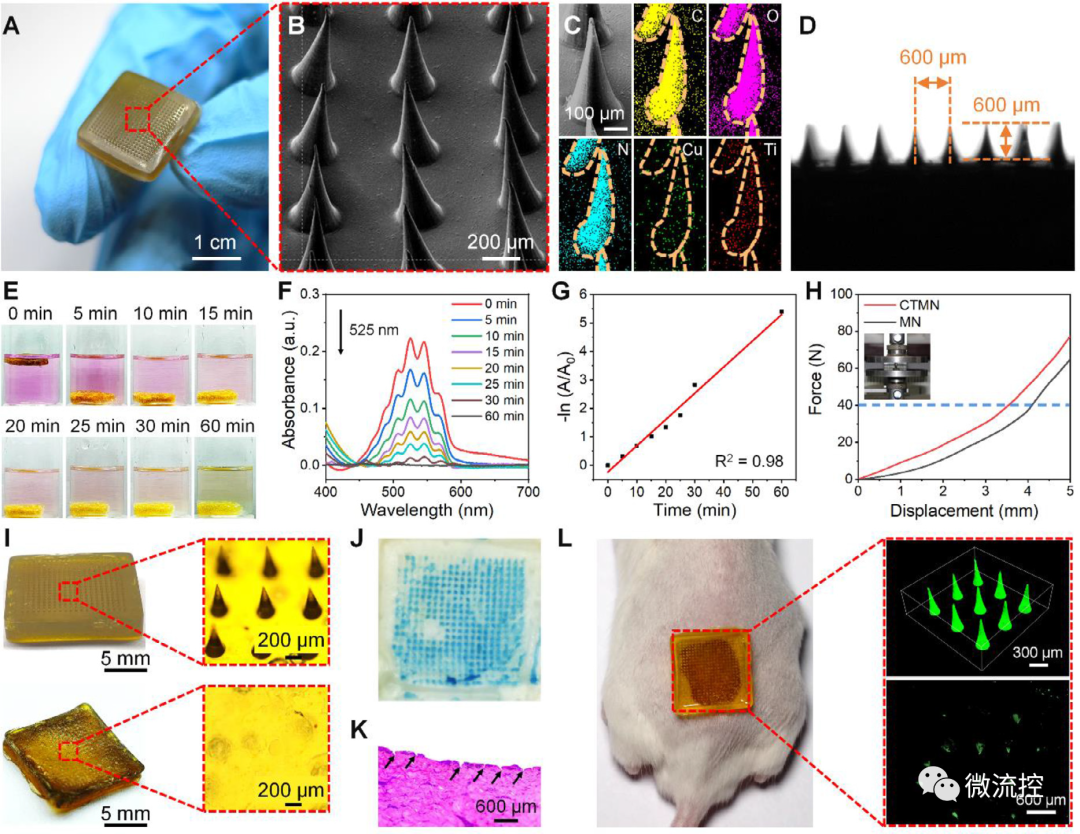
圖6 CuO?/TiO?微針(CTMN)的制備與表征
CTMN的體內治療性能
最后,研究人員構建了MRSA感染的小鼠傷口模型以檢測CTMN的體內抗菌活性(圖7)。將小鼠隨機分為四組:對照組、US組、CTMN組和CTMN + US組。紅外熱成像用于檢測不同治療后傷口溫度的變化。結果顯示CTMN + US組的傷口溫度升高到50℃,比對照組高25℃,并且周圍組織溫度略微升高。之后進一步證實了CuO?/TiO?已被代謝,未在體內積聚。進一步測定小鼠血清中炎癥因子水平,結果發現,CTMN + US組TNF-α和IL-6水平明顯低于其他各組,表明CTMN + US可有效改善炎癥反應。HE和Masson染色表明CTMN + US組無炎癥,表皮層形成完整,膠原沉積面積大,表明病變已愈合。總的來說,這些結果表明CTMN體內抗菌活性促進了傷口組織中瘢痕的形成和膠原蛋白的排列。
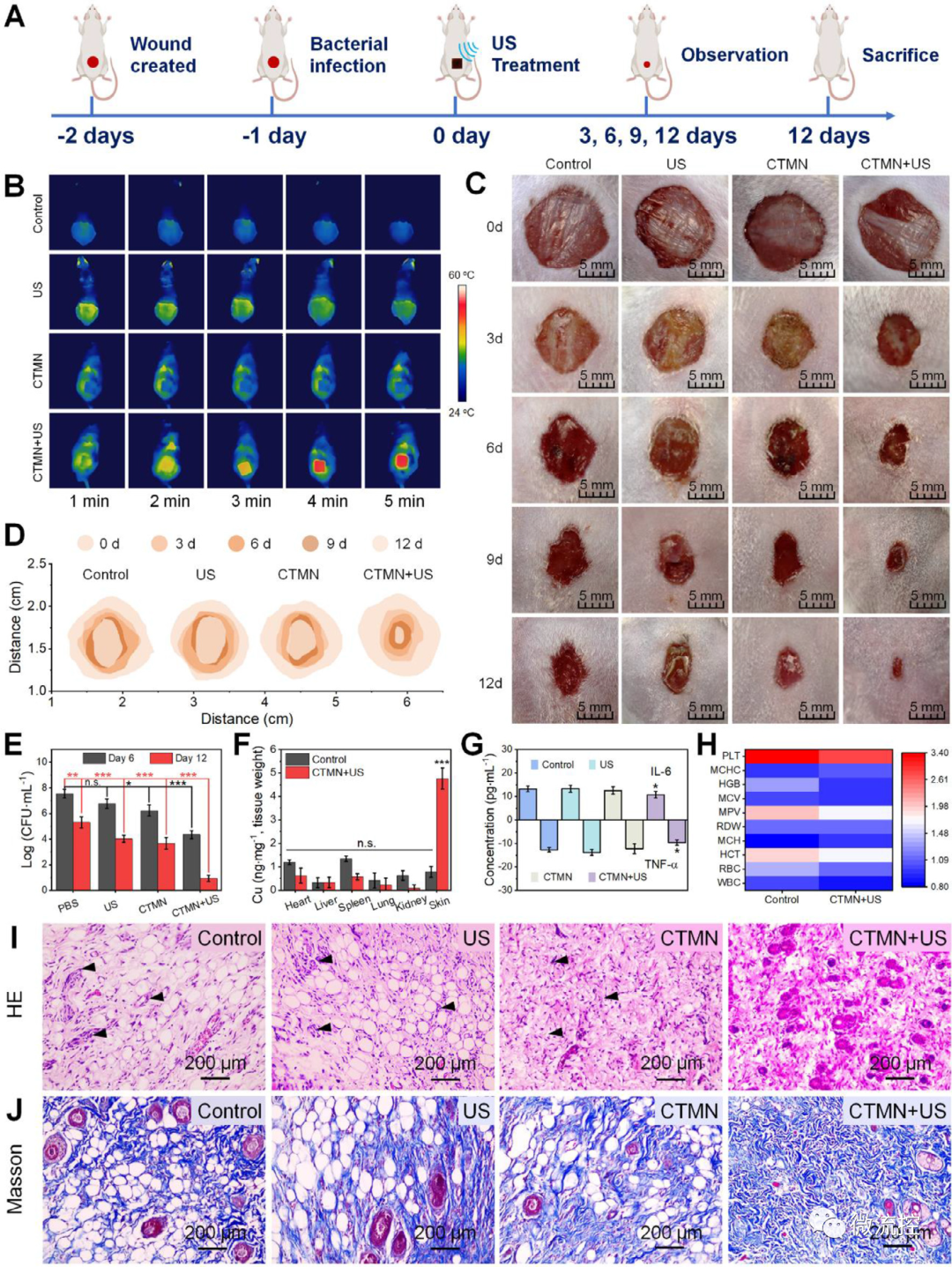
圖7 CTMN的體內治療性能
綜上,該研究開發了CuO?/TiO?集成微針,用于雙側增強聲化學動力學和超聲熱抗菌治療。通過材料表征、動力學測試、有限元模擬和DFT計算,研究了CuO?/TiO?的構效關系。經體外和體內實驗驗證,CTMN不僅在5 min內對多種MDR病原體的殺滅率為》 99.9999%,具有極高的抗菌效果,而且還能促進創面組織愈合。總的來說,這項工作開發了一種用于非抗生素治療的聲敏性和化學反應性納米藥物的潛在應用策略。
論文鏈接:
https://doi.org/10.1016/j.actbio.2022.12.041
審核編輯 :李倩
-
納米材料
+關注
關注
3文章
172瀏覽量
18902 -
催化劑
+關注
關注
0文章
93瀏覽量
10326 -
微針技術
+關注
關注
2文章
74瀏覽量
8720
原文標題:超聲激活微針貼片,用于雙側增強聲化學動力學和聲溫抗菌治療
文章出處:【微信號:Micro-Fluidics,微信公眾號:微流控】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
【Simcenter STAR-CCM+】通過快速準確的CFD仿真加速空氣動力學創新

使用Phase Lab鎳基動力學數據庫計算多組分合金的成分分布曲線
用于3D腦血管成像和腦血流動力學監測的可穿戴超聲貼片

“本源悟空”超導量子計算機助力大規模流體動力學量子計算

Simcenter STAR-CCM+車輛外部空氣動力學特性——通過快速準確的CFD仿真加速空氣動力學創新

掃描速率對各體系的電化學行為有什么影響
圓滿收官| Aigtek參展第二屆波動力學前沿與應用學術會議載譽歸來!

邀請函| Aigtek安泰電子攜經典產品,亮相第二屆波動力學前沿與應用學術會議!

高頻功率放大器模塊在聲化學誘導艾氏腹水瘤細胞研究的應用




 超聲激活微針貼片,用于雙側增強聲化學動力學和聲溫抗菌治療
超聲激活微針貼片,用于雙側增強聲化學動力學和聲溫抗菌治療










評論